Estrogeny należą do hormonów płciowych, które wpływają zarówno na kształtowanie się kobiecych narządów płciowych, jak i zawiadowanie cyklem miesięcznym czy funkcjami seksualnymi. Są one także zaangażowane w znacznie więcej „niehormonalnych zadań specjalnych” regulujących choćby funkcje układu odpornościowego, naczyniowego czy kostnego. Kluczowy jest jednak balans hormonalny (na osi estrogeny-progesteron), który pozwala na prawidłowe funkcjonowanie organizmu.
Co ciekawe, ostatnie lata badań nad mikrobiotą wskazują, że ważnym graczem w regulacji krążących estrogenów w ustroju jest estrobolom – czyli zestaw genów niektórych bakterii jelitowych, dzięki którym mogą one metabolizować estrogeny.
Jak dbać o dobrostan estrobolomu? Czy istnieje idealna dieta dla zdrowia hormonalnego?
Estrobolom, czyli mikrobiota zaangażowana w metabolizm estrogenów
Najprościej rzecz ujmując, estrobolom to agregat genów bakteryjnych, których produkty są zdolne do metabolizmu estrogenów. Oznacza to, że niektóre bakterie zamieszkujące nasze trzewia mają zdolność do produkcji enzymu nazywanego ß-glukuronidazą i za jego pośrednictwem wpływają na obrót estrogenów w ustroju. Ale zacznijmy od początku.
Estrobolom wpływa zarówno na wydalanie, jak i krążenie estrogenów w ustroju.
Estrogeny krążą we krwi w postaci wolnej lub związanej z białkami i wywierają różnorodne efekty biologiczne. W zależności od stanu fizjologicznego dominują różne formy estrogenów endogennych: estradiol (E2) dominuje u kobiet niebędących w ciąży przed menopauzą, estron dominuje po menopauzie, a estriol sprawuje władzę estrogenową u kobiet będących w ciąży [1].
Estrogeny podlegają efektowi pierwszego przejścia, co oznacza, że w pierwszej kolejności trafiają do wątroby, gdzie ulegają częściowemu metabolizmowi. I właśnie tutaj – w wątrobie ulegają reakcjom sprzęgania (tudzież koniugacji), co oznacza, że estrogeny przekształcane są do „skoniugowanych” metabolitów, które organizm może eliminować z ustroju z kałem i/lub moczem.
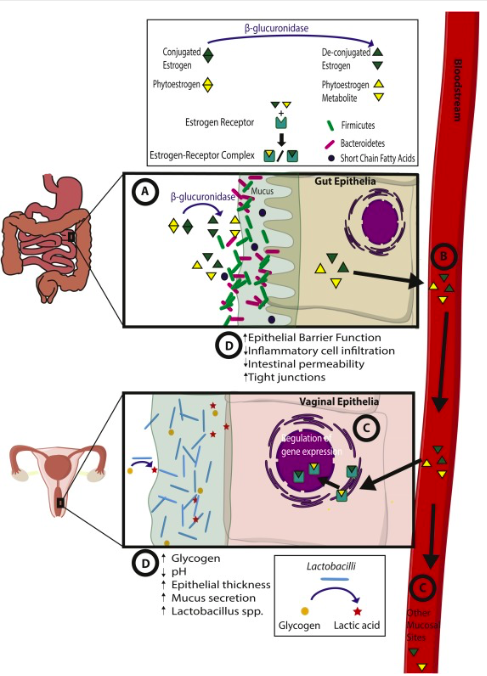
Warto jednak podkreślić, że takie skoniugowane estrogeny mogą być także wydalane z żółcią do światła przewodu pokarmowego i podlegać tzw. recyklingowi. I właśnie na tym etapie „cała na biało” wkracza mikrobiota jelitowa, która może ponownie odzyskiwać estrogeny trafiające z wątroby. Cały proces dzieje się za sprawą gatunków bakterii o aktywności ß-glukuronidazy. Umożliwia to ponowne wchłonięcie metabolizowanego estrogenu przez jelita i przeniesienie ich do krwiobiegu [2,3].
Warto podkreślić, że skład estrobolomu kształtują różne czynniki, między innymi:
- antybiotyki i inne leki (o wpływie leków na kształt mikrobioty jelitowej przeczytasz tutaj);
- dieta – im bardziej różnorodna i zasobna w nieprzetworzone pokarmy, tym bardziej różnorodna i „zdrowsza” mikrobiota;
- czynniki środowiskowe (stres, toksyny, alkohol);
- aktywność fizyczna (najlepiej iść w kierunku umiarkowanej aktywności);
- przewlekły stres (który negatywnie oddziałuje na mikrobiotę jelitową, a ponadto może prowadzić do dysbalansu między estrogenami a progesteronem).
Warto zatem przyjrzeć się zależności mikrobiota-estrogeny, bo coraz więcej badań wskazuje na potencjalny udział mikrobioty w rozwoju zaburzeń hormonalnych.
Dysbalans hormonalny, czyli o przewadze estrogenowej
Chociaż estrogen jest niezbędnym hormonem, jego zbyt wysokie stężenia w ustroju może zwiększać ryzyko niektórych chorób, w tym raka piersi i jajnika, a także endometriozy. Skąd się bierze i dlaczego rozwija się przewaga estrogenowa?
Warto nawiązać tutaj do czynników środowiskowych, które są „poza genetyką” i na które mamy realny wpływ. Dieta i styl życia w istocie mogą przekładać się na metabolizm estrogenów. Kolejny raz podkreśla się negatywny wpływ diety zachodniej na zdrowie, tym razem w kontekście promowania dominacji estrogenowej i ryzyka chorób związanych z nierównowagą hormonalną.
Badania wskazują, że wysokie spożycie przetworzonej żywności, słodyczy, rafinowanych zbóż, a także mięsa czerwonego wiążą się z wyższymi poziomami estrogenów. Jadłospis bazujący na żywności przetworzonej nierzadko powoduje nadwyżkę energetyczną, co w konsekwencji prowadzi do nadmiernej masy ciała i „sprzyja” przewadze estrogenowej [4].
Kolejna kwestia, o której warto wspomnieć, to nadmierna masa ciała. Estrogeny, poza nadnerczami i jajnikami, są produkowane także przez tkankę tłuszczową. Jej nadmierna ilość indukuje aktywność enzymu aromatazy, co przekłada się na podwyższone estrogeny. W kontekście nadwagi i otyłości także kolejny raz warto podkreślić rolę mikrobioty – dbałość o różnorodność ekosystemu jelitowego przekłada się na zdrowie metaboliczne. Badania wskazują, że osoby z nadmierną masą ciała mają zaburzone proporcje bakterii typu Firmicutes do Bacteroidetes. Obserwuje się tutaj większą liczbę bakterii typu Mollicutes, które mogą „efektywniej” pobierać kalorie z diety [5,6].
Ponadto dysbioza jelit i większy udział bakterii patologicznych w mikrobiocie powoduje większą gęstość naczyń włosowatych, co wpływa na wydajniejsze wchłanianie cukrów prostych. Sprzyja także zaburzeniom integralności bariery jelitowej, co sprzyja stanom zapalnym w ustroju. Więcej na ten temat pisałam tutaj.
Kobiety z nadwagą i otyłością wykazują trzykrotnie wyższe ryzyko zachorowania na raka piersi od kobiet o prawidłowej masie ciała.
Kolejną kwestią, o której warto wspomnieć w kontekście dominacji estrogenowej, jest narażenie na ksenoestrogeny, czyli substancje powszechnie występujące w codziennie przez nas stosowanych akcesoriach: lakierach do paznokci, dezodorantach, a także pestycydach stosowanych przy uprawie roślin. Ksenoestrogeny, wchodząc w interakcję z układem hormonalnym, oddziałują na receptory dla estrogenów i tym samym zaburzają jego pracę (nazywane są także: endocrine disruptors, co w wolnym tłumaczeniu oznacza substancje zaburzające gospodarkę hormonalną) [7].
Przewaga estrogenowa może być także wynikiem nieprawidłowo dobranej hormonalnej terapii zastępczej w okresie menopauzy (kluczowe jest optymalne dobranie dawki hormonów). Warto także wspomnieć o roli przewlekłego stresu, który promuje syntezę kortyzolu kosztem progesteronu (dochodzi do „efektu podkradania” pregnenolonu – wspólnego źródła dla produkcji kortyzolu i progesteronu).
Przewlekły stres prowadzi do nadmiernej produkcji kortyzolu kosztem progesteronu, który powstaje z tego samego prekursora.
Z przewagą estrogenową wiąże się także endometriozę – chorobę przewlekłą, w której dochodzi do „rozrostu” endometrium poza macicą. Jedno z badań wykazało, że mikrobiota może być ważnym ogniwem w całym procesie terapeutycznym – mikrobiota pacjentek cierpiących na endometriozę może zawierać dużą ilość bakterii dekoniugujących estrogeny, co może podbijać poziom estrogenów i wpływać na rozwój choroby. Oczywiście czynników zaangażowanych w etiopatogenezę choroby jest wiele (w tym aspekt genetyczny), aczkolwiek często podkreślane jest wsparcie przewodu pokarmowego, który odgrywa znaczącą rolę w metabolizmie estrogenów [8].
Mikrobiota, estrogeny i… zdrowie kości?
Chciałabym także nawiązać do przeciwstawnego efektu, mianowicie obniżonego poziomu estrogenów, ponieważ pojawiło się w tym temacie ciekawe badanie sugerujące ochronny wpływ interwencji probiotycznej na… zdrowie kości. Naturalnym stanem rzeczy, w którym następuje spadek poziomu estrogenów, jest okres menopauzalny, co zwiększa utratę gęstości mineralnej kości i zwiększa ryzyko złamań. Kluczowa w tym okresie jest dbałość o dietę, zawierającą odpowiednią ilość wapnia, magnezu (on też jest ważny dla zdrowia kości, wiąże się na powierzchni kryształów hydroksyapatytu, wpływając na większą elastyczność i mniejszą kruchość kości), a także regularną suplementację witaminą D (warto rozważyć przy tej okazji także witaminę K2. Więcej na ten temat przeczytasz w tym wpisie).
Jansson P.A. i wsp. przeprowadzili w 2019 ciekawe badanie, w którym wykazano, że określone szczepy probiotyczne mogą chronić przed utratą gęstości mineralnej kości, wywołaną niedoborem estrogenów. Badanie przeprowadzono na 249 zdrowych kobietach po menopauzie, które nie przyjmowały hormonalnej terapii zastępczej, a czas ostatniej miesiączki wynosił do 12 lat od włączenia do badania. Grupa badawcza otrzymywała probiotyk trzyszczepowy codziennie przez 12 miesięcy (szczepy, które były badane występują w preparacie Sanprobi Osteo), a grupa kontrolna placebo. Wyniki badania wskazały, że w grupie przyjmującej probiotyk odnotowano zmniejszenie utraty gęstości mineralnej kości w porównaniu do placebo. Co ciekawe, wpływ ochronny probiotyku na kości jest uzasadniony jego wspomaganiem bariery jelitowej, zwiększonym wydzielaniem krótkołańcuchowych kwasów tłuszczowych, zmniejszaniem stanu zapalnego i (!) obniżaniem cytokin prozapalnych w kościach. Powoduje to zmniejszoną aktywność osteoklastów (czyli komórek kościogubnych, które mają zdolność do „rozpuszczania” tkanki kostnej) i tym samym zmniejszoną resorpcję kośćca [9].
Po raz kolejny widzimy, że konkretne szczepy probiotyczne działają nie tylko lokalnie, ale oddziałują na funkcje całego ustroju (nawet pozornie niezwiązane z mikrobiotą jelit kości).
Dieta dla równowagi hormonalnej
Aktualne dane sugerują, że dla optymalnej pracy hormonów najkorzystniej wypada różnorodna dieta oparta na roślinach i bogata w błonnik (czyli znowu krążymy wokół modelu śródziemnomorskiego), z kolei dieta zachodnia daje przeciwstawne wyniki. W jednym z badań przeglądowych (gdzie uwzględniono ponad 30 badań) wykazano, że model diety zachodniej był związany z czternastoprocentowym wzrostem ryzyka raka piersi. Z kolei dieta obfitująca w warzywa i owoce zmniejszała to ryzyko o 18% [10].
Ciekawe obserwacje dotyczą też diet wegetariańskich w kontekście poziomu estrogenów w ustroju. W amerykańskim badaniu porównano 10 kobiet przed menopauzą stosujących „zachodnią dietę”, która zawierała wysoką zawartość tłuszczu (40% kalorii) i niską zawartość błonnika, z 10 wegetariankami w tym samym wieku spożywającymi dietę bogatą w błonnik i umiarkowaną zawartość tłuszczu (30%). Aktywność β-glukuronidazy bakteryjnej w kale była istotnie statystycznie niższa u wegetarianek niż u pań jedzących wszystko, a wegetarianki potroiły poziom estrogenów w kale i odnotowały 15- 20% niższy poziom estrogenów w surowicy w porównaniu do osób na diecie klasycznej [1].
Obecność błonnika jest również kluczowa, poprawia pasaż i motorykę jelit, wspierając eliminację estrogenów z kałem.
Poza różnorodnymi warzywami i owocami w diecie, a także bazowaniu na nieprzetworzonej żywności (zbożach pełnoziarnistych, strączkach, orzechach i pestkach, zdrowych tłuszczach) a ograniczeniu mięsa, cukrów prostych i jedzenia przemysłowego) należy szczególnie zadbać o odpowiednią podaż witamin z grupy B, które są kluczowe dla prawidłowej gospodarki hormonalnej. To kolejny ważny składnik dla prawidłowego metabolizmu estrogenów. W wątrobie w metabolizm estrogenów zaangażowany jest enzym COMT (katecholo-O-metylotransferaza), której kofaktorem jest właśnie magnez. Ponadto wysoki poziom estrogenów w ustroju „wyczerpuje” zapasy magnezu, a przy ogólnych tendencjach (statystycznie spożywamy za mało magnezu z dietą) być może warto wdrożyć przemyślaną suplementację tym pierwiastkiem [11].
Magnez jest kluczowy dla prawidłowego metabolizmu estrogenów w wątrobie, ponadto wpływa na prawidłowe przyswajanie witaminy D oraz dba o prawidłowe wydzielanie neuroprzekaźników: dopaminy, noradrenaliny, a także kortyzolu.
Podsumowanie
Dbałość o różnorodną mikrobiotę jelitową okazuje się mieć kolejny wymiar zdrowotny, tym razem w kontekście zdrowia hormonalnego. Przewaga estrogenowa może prowadzić do różnych nieprzyjemnych objawów, a także być zaangażowana w rozwój chorób przewlekłych (endometrioza) czy nowotworów piersi.
Jakich zaleceń należy przestrzegać, aby wspierać gospodarkę hormonalną?
- Postaw na nieprzetworzoną dietę, zasobną w produkty roślinne oraz błonnik, np. dietę śródziemnomorską. Ogranicz przetworzone, czerwone mięso, cukry proste i rafinowane węglowodany.
- Dbaj o regularne ćwiczenia i aktywność fizyczną, która wesprze w zachowaniu prawidłowej masy ciała. Nadmierna ilość tkanki tłuszczowej wpływa na zwiększoną produkcję estrogenu w ustroju.
- Warto zadbać o przestrzeganie rytmu okołodobowego, dobrej jakości sen i radzenie sobie z sytuacjami stresowymi. Łatwo się pisze, ale gorzej się z tym w rzeczywistym świecie zmierzyć. Niemniej jednak warto o tym pamiętać i włączać w miarę możliwości praktyki relaksacyjne.
- Zadbaj o prawidłową podaż magnezu, zdrowych tłuszczów omega-3 i witaminy D. To ważne ogniwa dla prawidłowych funkcji hormonów.
Wszystkie te punkty będą także wpływały na skład i różnorodność mikrobioty jelitowej. Pamiętajmy też, że wsparciem ekosystemu jelitowego może być czasowa, przemyślana suplementacja probiotyczna preparatami wieloszczepowymi, która będzie uzupełnieniem powyższych działań.
Jeżeli masz ochotę obejrzeć ten materiał w formie video z moim gościem mgr Emilią Cesarek- zajrzyj na Instagram.
Artykuł powstał we współpracy merytorycznej z partnerem Sanprobi.
Bibliografia:
[1] Kwa M, Plottel CS, Blaser MJ, Adams S. The Intestinal Microbiome and Estrogen Receptor-Positive Female Breast Cancer. J Natl Cancer Inst. 2016;108(8):djw029. Published 2016 Apr 22
[2]Gloux K, Berteau O, El Oumami H, Beguet F, Leclerc M, Dore J. A metagenomic beta-glucuronidase uncovers a core adaptive function of the human intestinal microbiome. Proc Natl Acad Sci U S A. 2011;108
[3]Dabek M, McCrae SI, Stevens VJ, Duncan SH, Louis P. Distribution of beta-glucosidase and beta-glucuronidase activity and of beta-glucuronidase gene gus in human colonic bacteria. FEMS Microbiol Ecol. 2008;66(3):487–495.
[4] Sánchez-Zamorano LM, Flores-Luna L, Angeles-Llerenas A, Ortega-Olvera C, Lazcano-Ponce E, Romieu I, Mainero-Ratchelous F, Torres-Mejía G. The Western dietary pattern is associated with increased serum concentrations of free estradiol in postmenopausal women: implications for breast cancer prevention. Nutr Res. 2016 Aug;36(8):845-54.
[5] Mair KM, Gaw R, MacLean MR. Obesity, estrogens and adipose tissue dysfunction – implications for pulmonary arterial hypertension. Pulm Circ. 2020;10(3):2045894020952019. Published 2020 Sep 18. doi:10.1177/2045894020952023
[6] Pokrzywnicka P, Gumprecht J. Intestinal microbiota and its relationship with diabetes and obesity. Clin Diabetol 2016; 5, 5: 164–172.
[7] Roy JR, Chakraborty S, Chakraborty TR. Estrogen-like endocrine disrupting chemicals affecting puberty in humans–a review. Med Sci Monit. 2009 Jun;15(6):RA137-45.
[8] Laschke MW, Menger MD. The gut microbiota: a puppet master in the pathogenesis of endometriosis? Am J Obstet Gynecol. 2016 Jul;215(1):68.e1-4. doi: 10.1016/j.ajog.2016.02.036. Epub 2016 Feb 18.
[9] Jansson P-A. et al. Probiotic treatment using a mix of three Lactobacillus strains for lumbar spine bone loss in postmenopausal women: a randomised, double-blind, placebo-controlled, multicentre trial; The Rheumatology 1(3):e154-e162
[10] Xiao Y, Xia J, Li L, et al. Associations between dietary patterns and the risk of breast cancer: a systematic review and meta-analysis of observational studies. Breast Cancer Res. 2019;21(1):16. Published 2019 Jan 29.
[11] Bastos P, Araújo JR, Azevedo I, Martins MJ, Ribeiro L. Effect of a natural mineral-rich water on catechol-O-methyltransferase function. Magnes Res. 2014 Jul-Sep;27(3):131-41.


